С6н6сl6 |
|
Скачать презентацию |
||
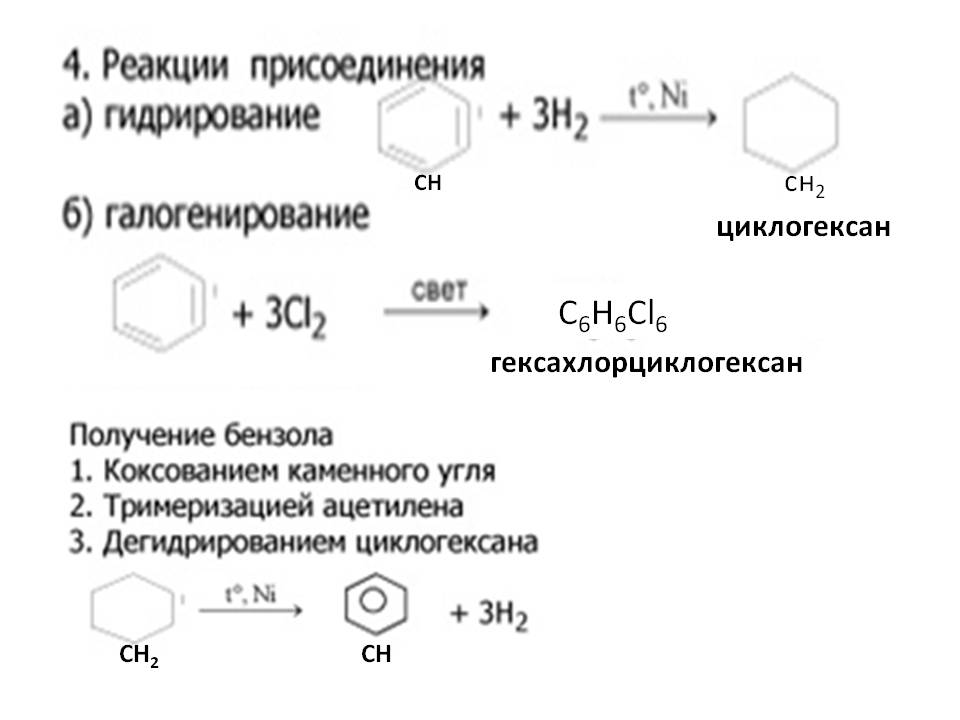
| << Из реакций галогенирования наибольшее значение имеют хлорирование и | Задания для зачета: В.1: а) Строение этилена >> |
Скачать презентацию
Химия 10 класс
краткое содержание других презентаций«Генетическая связь» - Генетическая связь между основными классами неорганических соединений. Б). Основания. Na3PO4. Составьте уравнения реакций. Составьте уравнения химических реакций, расставьте коэффициенты. H2O. Простые. Al(NO3)3. =. Неметаллы. Проверьте правильность составления схемы. В). Кислота. Основание. Составьте уравнение реакции.
«Химия Алканы» - Д.з. :№3, упр.8, в-сы 9,10,11. Получение алканов. (Пром. получение ацетилена). Р. Применение. МОУ СОШ № 5 г. Светлого. Урок №4 Химические свойства алканов.
«Кристаллы» - Кристаллы. Кристаллы - природные многогранники. Лазер светит ярче тысячи солнц. Кристаллы растут из паров, расплавов и вырастают в виде удивительно правильных многогранников. Выяснить: Как возникли кристаллы? Оказалось, что кристалл рубина усиливает свет.
«Химия мыла» - Исполнитель: ученица 10 А класса Перелётова Дарья Романовна. Вредные вещества. Триэтаноламин Диэтиленгликоль. Кокосовое и пальмовое масло Глицерин Соли натрия. Таблица выводов. Проект: «…Да здравствует мыло душистое!». Химические свойства. Тип проекта: исследовательский. Исследуемое мыло. Общий вывод. Физические свойства. Руководитель: учитель химии Александрова Татьяна Владимировна. Полезные вещества.
«Ломоносов и химия» - Корпускулы, состоящие из нескольких первичных, и притом различных, называются производными. Итак, смешанное тело состоит из производных корпускул. В течение многих лет химия являлась основным занятием Ломоносова. Здешние химики сие изобретение за превеликое дело почитают». «Элементы математической химии». Но и Кункель унёс в могилу свою тайну. Знаменитые мозаики М.В. Ломоносова. Вывод 6. Музей М. В. Ломоносова. В химической лаборатории Ломоносов провёл более 4-х тысяч опытов! Аналогичны соображения о принципе сохранения вещества, показывающего несостоятельность теории теплорода.
«Амины» - Амид – является продуктом замещения гидроксильной группы на остаток амина. Первичные и вторичные амины способны образовывать водородные связи. Первичный амин метиламин Вторичный амин деэтиламин Третичный амин триэтиламин. Ион аммония. Изомерия положения функциональной группы: Выступая в роли нуклеофилов: Строение. Первичный амин прапиламин. Амины. Химические свойства. Остальные низшие амины – жидкости, которые хорошо растворяются в воде. Образуя Амиды – важнейший класс органических соединений:
Всего в теме «Химия 10 класс» 59 презентаций