Последствия загрязнения воздуха |
|
Скачать презентацию |
||
| << Парниковый эффект | Экологическое состояние в округах Москвы >> |
Скачать презентацию
Химия 8 класс
краткое содержание других презентаций«Урок Кислород» - Купцова А.А.Методическая разработка урока по химии «Кислород. Выпуск 2./Под общей редакцией Н.В.Борисовой. – Чебоксары, 2010. – 208 с.). Цели : Предисловие. ИКТ оказывает большую помощь также при подготовке и проведении уроков. Нахождение в природе. Поэтому работа с учащимися требует от учителя постоянного методического технического совершенствования. Готовлю презентации к урокам, чтобы разнообразить формы уроков химии учащихся. В предлагаемой методической разработке представлена разработка урока «Кислород.
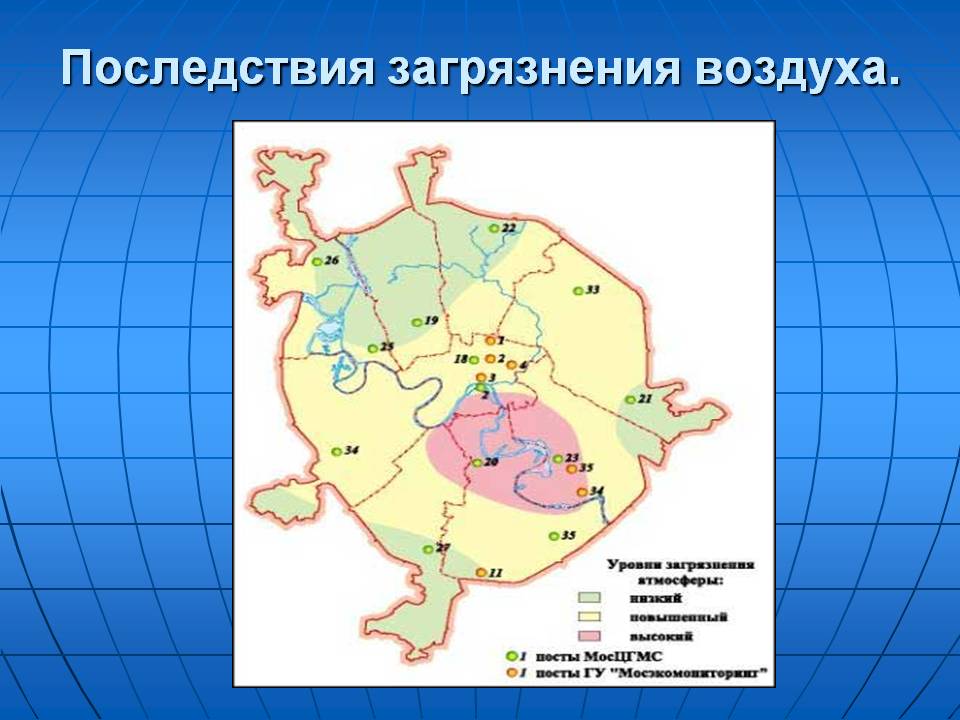
«Воздух химия» - Состав воздуха. Последствия загрязнения воздуха. Основные загрязнители воздуха. Экологическое состояние в округах Москвы. Автомобильные выхлопы, выбросы промышленных предприятий. Карта глобального потепления. Озоновые дыры. Определить основные пути решения проблемы загрязнения воздуха. Кислород- 20,8% Аргон- 0,93% Азот- 78,2 % Прочие газы- 0,07%. Переменные составные части воздуха. Парниковый эффект. Цели и задачи.
«Элементы металлы» - Покажите как распределяются электроны в атомах гелия и неона. Проверка домашнего задания. Цели урока: Инертные газы Каждая молекула инертного газа состоит из одного атома. 1. Где в периодической системе находятся элементы, соответствующие простым веществам металлам? Аллотропия кислорода. 2. Каковы общие физические свойства металлов? (Белый фосфор). He - Ne - Ar - Kr - Xe - Rn -. Благородные газы: Применение гелия, неона и аргона. Изучение новой темы.
«Оксиды 8 класс» - Al2O3. H2CO3. Горный хрусталь. Углекислый газ. SO2. Речной песок. Н2o. Важнейшие классы неорганических веществ. Негашеная известь. Кварц. «Крестики-нолики». Na2SO4. K3PO4. Соль. Вода. Сапфир. Рубин. H2S. Основание. FeO. Оксид. Корунд. Речной песок, кварц, аметист, горный хрусталь. Оксиды. HNO3. Аметист. H2SiO3. MgO. Al(OH)3. Сaco3. Al(NO3)3. CO2. Ca(OH)2. Распределить вещества по строению на 4 группы.
«Сложные и простые вещества» - Например, атомы кремния и кислорода объединяются в кристаллы кварца. Сложные вещества, как и простые, имеют молекулярное ,так и немолекулярное строение. Образование сложного вещества из простых называется синтезом. Над презентацией работала Патокина Юлия ученица 8-б кл. Исключение составляют медь(красного цвета) и золото(жёлтого цвета). Большинство металлов обладают серым, серебристо- белым цветом. В сложных веществах объединяются атомы различных элементов. Сложные вещества.
«Металлы и неметаллы» - II Стадия «Осмысление». Приём: «Сводная таблица». ? I Стадия «Вызова». Сравнение характеристик простых веществ – металлов и неметаллов. ТЕМА УРОКА: «Аллотропия». Стадия «Рефлексия». Работа ведется в группах. ! Второй вариант. III. I. Стадия «Вызова» Найдите ошибку в синквэйне:
Всего в теме «Химия 8 класс» 53 презентации