Алкадиены химия |
|
Химия 9 класс
Скачать презентацию |
||
| << Углеводороды ряда этилена | «Жиры» химия >> |
Химия 9 класс
краткое содержание других презентаций«Галогены химия» - Биологическая роль фтора. Физические свойства. ПРОЕКТ «Галогены. Опыт 1. Доказательство наличия фтора в данной зубной пасте. Растворяет отложения на суставах. Способствует избавлению от лишнего веса. Открытие галогенов. Выводы и рекомендации. В школьной библиотеке. Литература. Содержание йода в виде различных соединений в организме человека составляет 25—30 мг.
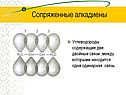
«Алкадиены химия» - Крайний атом С-Sp2-гибридизация. Сопряженные алкадиены. Алкадиены: строение,номенклатура,гомологи,изомерия. Схема строения аллена. Алкадиены с кумулированным расположением двойных связей. Алкадиены с изолированными двойными связями. Номенклатура алкадиенов. Актуализация ранее полученных знаний. Игра. Урок химии в 9 классе Учитель: Дворничена Л.В. Центральный атом С-Sp3-гибридизация.
«Металлы в химии» - Металлы. 1.С кислородом 2.С галогенами 3.С водородом 4.С серой 5.С азотом. Пайке Обтачиванию Сверлению Пилению Строганию Обработке на станках и др. Металлическая связь. Взаимодействие со сложными веществами. Презентация подготовлена учителем химии Рощепкиной Н. А. для параллелей 9-х и 11-х классов. Металлический блеск (кроме йода.
«9 класс Алюминий» - AL. Химические свойства алюминия. С серной и азотной концетрированными не реагирует. Неметаллы. Физические свойства алюминия. Взаимодействует: 1.С неметаллами (с кислородом). Положение алюминия в периодической системе Д.И.Менделеева. Амфотерность алюминия. 2AL+ 2NaOH + 2H2O=2NaALO2 +3H2. 4AL +3O2 =2AL2O3. 2AL+6HCL=2ALCL3 +3H2. Металлы. 4.С оксидами металлов (алюминотермия). Урок химии в 9 классе по теме «Алюминий».
«Азот химия» - Цели: Содержит на внешнем энергетическом уровне 5 электронов +7 ) ) 2 5. К.Шееле и Г.Кавендиш получили азот Д.Резерфорд описал получение и свойства 1787г. Li3N, Ca3N2, AlN, H3N N2O, NO, N2O3, NO2, N2O5. Рассмотреть физические и химические свойства азота в свете ОВР. Показать значение азота как биогенного элемента. Строение и свойства атома. Восстановитель N0 –1,2,3,4,5e- ? N+1,N+2,N+3,N+4,N+5 * Составьте формулы оксидов. 3. Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №5.
«Развитие органической химии» - Демонстрации. Итоговое тестирование. Знания об органических веществах у древних людей. Контрольная работа. Структурная теория. Защита творческого проекта. Зачёт. Итоговая конференция. Зачётный практикум. Штрубе В. Пути развития химии. Проследить эволюцию химических идей и представлений в период от предыстории до настоящего времени. Семинары. Тематическое планирование. Решение расчётных и экспериментальных задач по органической химии. Программа курса.
Всего в теме «Химия 9 класс» 94 презентации